في أكتوبر/تشرين الأول من عام ٢٠١١، أعلنت لجنة نوبل اسم العالم الكندي رالف ستاينمان ضمن الفائزين بنوبل الطب، تقديرا لاكتشافه الخلايا المتغضنة ودورها في المناعة. لكن إعلان فوزه بالجائزة كان له طابع فريد من الحزن والدهشة، حيث جاء بعد ثلاثة أيام فقط من وفاته. فبينما كانت لجنة نوبل تعلن اسمه كفائز، لم تكن تعلم أنه قد فارق الحياة متأثرا بمرض سرطان البنكرياس.
ووفقا لقوانين مؤسسة نوبل، لا تمنح الجائزة بعد الوفاة، لكن اللجنة قررت إبقاء قرارها بعد مداولات، معتبرة أنه تم "بنية حسنة" قبل معرفة وفاة ستاينمان. ومما أضاف إلى درامية الموقف، هو ما ذكرته ابنته، حيث كان ستاينمان يمزح مع عائلته قبل أسبوع من وفاته بأنه يجب أن يبقى على قيد الحياة حتى إعلان الجائزة لأنها لا تمنح للمتوفين.
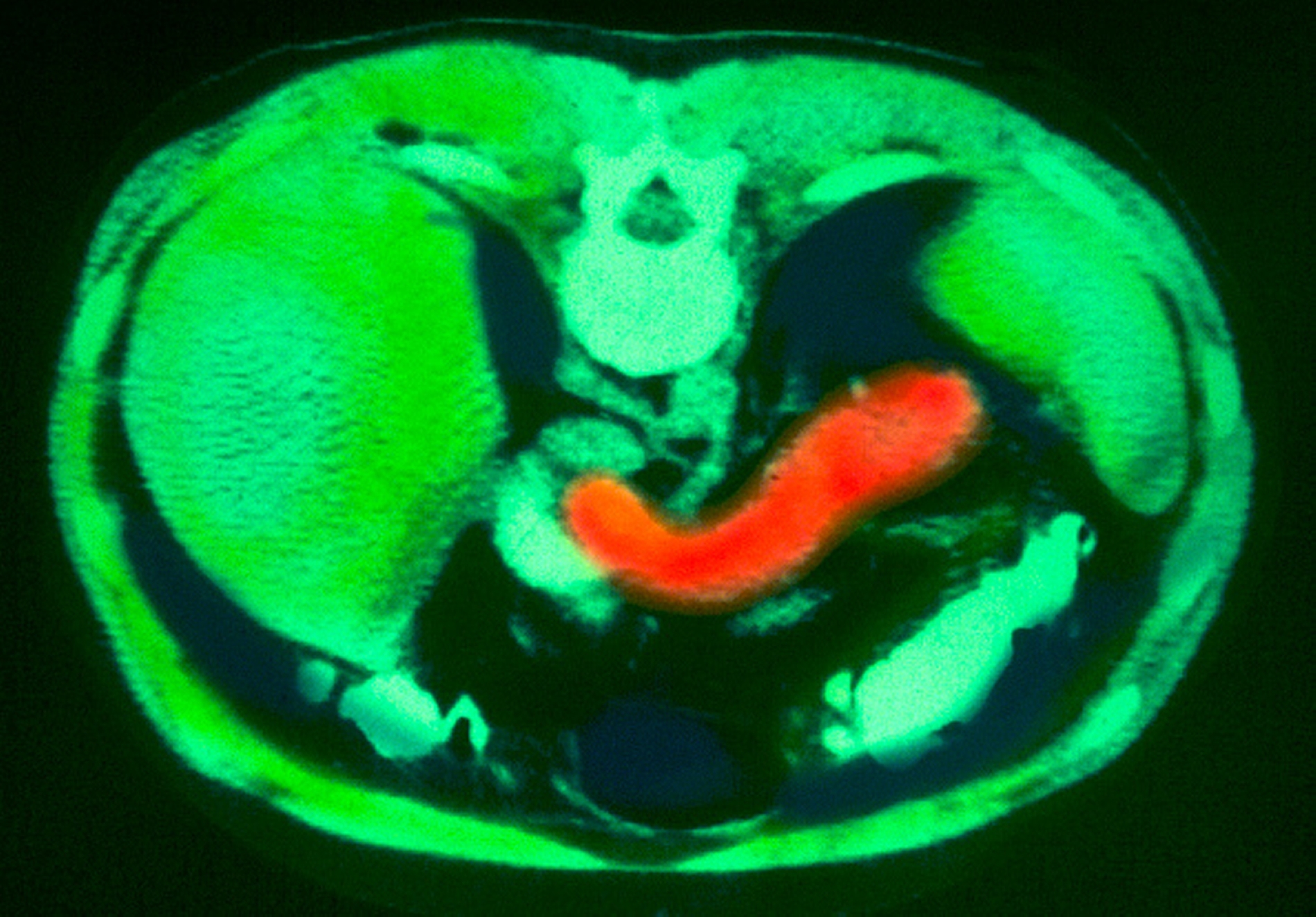
يعرف سرطان البنكرياس بسمعته القاسية، فهو من أكثر الأورام فتكا ومقاومة للعلاج، وغالبا ما يأتي تشخيصه متأخرا، بينما تفشل العلاجات المناعية التي أثبتت فعاليتها في سرطانات أخرى في إحداث فرق ملموس معه.
لكن دراسة حديثة نُشرت في مجلة "ساينس إيميونولوجي" قدمت بصيص أمل جديدا، حيث كشفت عن استراتيجيا علاجية مزدوجة تقوم على تنشيط الخلايا المتغصنة، وهي تلك الخلايا التي اكتشفها ستاينمان الذي توفي جراء النوع نفسه من السرطان.
الخلايا المتغصنة
حين نتحدث عن جهاز المناعة، غالبا ما يتبادر إلى الذهن صورة الخلايا القاتلة التي تهاجم البكتيريا والفيروسات أو تدمر الخلايا السرطانية. لكن قبل أن تبدأ أي معركة مناعية، هناك جنود مجهولون يعملون بصمت، مهمتهم ليست القتال، بل التعليم والإرشاد. هؤلاء هم الخلايا المتغصنة، التي تلقب أحيانا بـ"مدربي المناعة"، لأنها تعرف الخلايا الأخرى الى هوية العدو، وتضع خريطة الطريق لأي هجوم ناجح.